Boli Inflamatorii Intestinale
Bolile inflamatorii intestinale sunt afecțiuni cronice ale tubului digestiv, de cauză necunoscută. Termenul de “boli inflamatorii intestinale cronice” include colita ulcerativă (CU), boala Crohn (BC) și colita nedeterminată (5-15% din cazuri în care diferențierea între CU și BC nu se poate face pe baza criteriilor convenționale de diagnostic).
Incidența BC este de 5-10/100.000 locuitori pe an iar prevalența este de 50-100/100.000 în țările Europei de Vest și Americii de Nord. Incidența CU în aceleași țări este de 6-8/100 000 de locuitori iar prevalenţa 70-150/100.000. În Europa de Est și în România, incidența și prevalența ambelor boli inflamatorii este mai mică, dar cu tendință de creștere în ultima perioadă. Aceste diferențe între regiunile geografice sunt explicate de originea etnică, de stilurile de viață și alimentație distincte. Raportul între sexe este aproximativ egal, cu o ușoară predominanță feminină în cazul BC.
BC este diagnosticată cel mai frecvent la persoane între 15 și 30 de ani, deși vârsta la care poate debuta boala poate varia. Există un al doilea vârf al incidenței bolii situat în decada a 7-a. CU poate debuta la orice vârstă, dar diagnosticul înaintea vârstei de 5 ani sau peste 75 de ani este cu totul excepțional. Vârful de incidență se încadrează în decadele a doua si a treia, cu un al doilea vârf al incidenței, mai mic comparabil cu BC, la vârsta de 60-70 de ani.
Factorul declanșator al bolilor inflamatorii intestinale este încă necunoscut. Au fost incriminați factori genetici, infecțioși, imunologici și de mediu.
Factori genetici
Rolul predispoziției ereditare a fost demonstrat prin apariția mai frecventă a bolii în familiile în care există membri afectați. Studii statistice au identificat incidența crescută a bolii la anumite populații (rasa albă și în special la evrei) și la gemenii monozigoți.
Factori infecțioși
Deși nu s-au evidențiat cu certitudine până în prezent microorganismele implicate în apariția bolilor inflamatorii intestinale, majoritatea autorilor aduc în discuție rolul bacteriilor florei intestinale endogene sau al diferiților agenți infecțioși patogeni (Chlamidia, Listeria monocytogenes, Pseudomonas, Mycobacterium paratuberculosis, virusuri). Rolul virusurilor în declanșarea puseelor inflamatorii intestinale este susținut de acutizarea bolii la copii după infecții virale sau cu mycoplasme.
Factori imunologici
Dezechilibrele în imunitatea umorală sau celulară pot determina apariția bolii. Un argument în acest sens îl constituie posibila asociere a manifestărilor extradigestive cu caracter autoimun (artrită, colangită etc.) care se remit sub tratament cortizonic sau cu imunosupresoare și se corelează cu creșterea nivelului seric al complexelor imune circulante.
Factori de mediu
Fumatul, unul dintre factorii de risc intens studiați, este mult mai frecvent în rândul pacienților care dezvoltă BC și în special la cei care sunt supuși intervențiilor chirurgicale. Din contră, incidența colitei ulcerative este mai mare la nefumători. Mecanismele sunt incomplet elucidate.
Poate să afecteze orice segment al tubului digestiv pe o porțiune variabilă, dar se localizează cu predilecție la nivelul ileonului terminal și colonului.
Macroscopic, afectarea este discontinuă, segmentele interesate sunt separate de zone de aspect normal. Zonele intestinale afectate sunt îngroșate și pot atinge o grosime de până la 1 cm, prin congestie, hemoragie intraparietală și edem. Lumenul intestinal este îngustat pe distanțe variabile. Plăcile Peyer se îngroașă și apar adenopatii mezenterice. În faza acută a bolii apar ulcerațiile focale, care cu timpul capătă aspecte serpiginoase și pot ajunge la nivelul seroasei. Mucoasa dintre ulcerații este normală și datorită alternanței zonelor lezate cu zone normale se realizează aspectul de „pietre de pavaj”. În faza cronică peretele intestinal se îngroașă, devine rigid, cu lumenul îngust, asemănător unui furtun. Mezenterul din jur este scleros și retractil, iar ganglionii mezenterici sunt măriți de volum. Extensia procesului inflamator prin fistule în organele din jur, realizează conglomerate pseudotumorale.
Microscopic, apare edem și infiltrat inflamator în toate tunicile peretelui. Țesutul limfoid local prezintă hiperplazie marcată. Infiltratele inflamatorii sunt inițial formate din polimorfonucleare dispuse subepitelial, apoi infiltrează criptele cu formare de microabcese. Prin evacuarea microabceselor, se formează ulcerațiile. Ulcerațiile pot fi superficiale și profunde, și pot atinge toate straturile peretelui intestinal. Cele profunde se însoțesc de formarea de fistule deschise în alte anse intestinale, în vezica urinară, la tegument, ombilic sau perineu. În faza cronică apar infiltrate inflamatorii caracteristice, cu aspect de granuloame, care interesează toată grosimea peretelui intestinal. Acestea sunt formate din limfocite, plasmocite, eozinofile și celule gigante multinucleate. Aspectul este asemănător cu cel al granuloamelor din sarcoidoză. Necroza de cazeificare este absentă.
În faza acută a bolii modificările se localizează numai la nivelul mucoasei colonului. Macroscopic aceasta apare hiperemică, edemațiată, cu eroziuni punctiforme și foarte friabilă. Inflamația este continuă fără intervale de mucoasă sănătoasă. Microscopic se constată alterarea arhitecturii criptelor glandulare. Leziunea anatomopatologică, caracteristică CU în forma acută este abcesul criptic care apare prin necroza epiteliului glandular cu degenerescența celulelor epiteliale și apariția unui infiltrat inflamator cu polimorfonucleare, limfocite și plasmocite.
În faza subacută ulcerațiile epiteliului glandular coexistă cu procesele reparatoare, regenerative. Insulele de regenerare ale mucoasei înconjurate de zone de ulcerație și de mucoasă denudată apar ca proeminențe în lumenul colonului și realizează pseudopolipi de natură inflamatorie.
În faza de remisiune aspectul macroscopic este de cele mai multe ori normal. Microscopic se constată atrofia mucoasei glandulare și absența infiltratului inflamator. Țesutul fibros înlocuiește zonele distruse, glandele sunt deformate și lipsește secreția de mucus.
Tabloul clinic al BC este heterogen și include dureri abdominale, diaree și scădere ponderală. Debutul este extrem de variabil, de obicei lent, insidios, cu manifestări nespecifice care pot întârzia diagnosticul cu luni sau ani de zile. Pacienții se pot prezenta cu stare generală alterată, febră (38-39oC) și astenie fizică. Ocazional, când boala este mai extinsă la nivelul intestinului subțire sunt prezente manifestări de malabsorbție care, asociate anorexiei și efectelor catabolice ale procesului inflamator cronic, determină scăderea ponderală marcată. În interesarea gastrică sau duodenală pacienții pot prezenta un sindrom clinic ulceros cu epigastralgii postprandiale sau dureri în etajul superior care pot mima o suferință pancreatică. În unele situații debutul BC poate fi brutal printr-o complicație care domină tabloul clinic și necesită diferențierea de afecțiuni chirurgicale:
• debutul acut cu febră, dureri în fosa iliacă dreaptă și leucocitoză poate mima apendicita acută (la acești pacienți laparatomia evidențiază ileonul terminal tumefiat, de culoare roșie și consistență moale cu ganglionii regionali hipertrofiați);
• la 20-30 % din pacienți debutul se face prin ocluzie intestinală determinată de inflamația și edemul segmentului intestinal afectat;
• la unii pacienți, boala poate fi obiectivată datorită unei fistule cutanate, unui abces peri-anal, sau unei fistule enterovezicale cu infecție urinară secundară;
• în foarte rare cazuri debutul poate fi brutal cu semne de peritonită generalizată cauzată de perforația intestinală.
Sunt manifestări comune ale caracterului transmural al bolii. Fistulele perianale sunt cele mai comune, estimate la 15-35% dintre pacienți. De cele mai multe ori acestea sunt autolimitate și se pot vindeca fie de la sine, fie prin îngrijirea locală a pacientului, ceea ce poate întârzia mult diagnosticul. Există și situația când multiple traiecte fistuloase se unesc și formează o rețea cu mai multe orificii la nivelul regiunii perianale inclusiv labiile sau scrotul. Fistulele entero-enterice, entero-colice sau colo-colice sunt de cele mai multe ori asimptomatice. Dacă traiectul fistulos interceptează duodenul sau stomacul pacienții pot prezenta vărsături cu aspect fecaloid. Fistulele recto-vaginale pot apărea prin inflamația excesivă a peretelui anterior al rectului. Sunt mai frecvente la femeile care au suferit histerectomie în antecedente. Clinic pot fi observate scurgeri vaginale sau chiar emisie de scaun transvaginal. Fistule entero-vezicale sau colo-vezicale pot fi evidențiate la pacienții cu infecții urinare polimicrobiene persistente sau chiar fecalurie. Fistulele entero-cutanate care se deschid la nivelul abdomenului anterior apar de obicei după intervențiile chirurgicale. O situație aparte o constituie fistula postapendicectomie, atunci când diagnosticul de BC este confundat cu o apendicită acută. Studiile clinice estimează faptul că aproximativ un sfert dintre pacienți vor prezenta un abces intra-abdominal pe parcursul evoluției bolii. Simptomatologia clasică include febra, durerea abdominală cu sensibilitate la palpare sau semne de iritație peritoneală localizată. Majoritatea pacienților cu risc de abcese sunt în tratament cortizonic ceea ce maschează mult simptomatologia și îngreunează diagnosticul precoce.
Stricturile fac parte din tabloul clinic al BC și pot apărea în orice segment în care inflamația a fost suficient de puternică și îndelungată. De obicei se localizează la nivelul anastomozelor la pacienții care au suferit rezecții intestinale, fiind foarte multă vreme asimptomatice. Când lumenul este suficient de îngust apar dureri colicative postprandiale, balonare și în final ocluzie completă. Diagnosticul diferențial al stricturilor permanente, fibroase față de cele produse de inflamație, edem și spasm se face cu dificultate. Administrarea de glucagon care relaxează temporar musculatura striată poate fi utilă.
• cutaneo-mucoase: eritem nodos, stomatită aftoasă, leziuni nodulare ulcerate
• oculare: irită, uveită, episclerită
• osteo-articulare: artrite enteropatice, hippocratism digital, osteomielită pelvină, osteomalacie prin sindrom de malabsorbție cu deficit de calciu și vitamina D
• hepatobiliare: hepatită autoimună, colangită sclerozantă
Elementele esențiale care realizează tabloul clinic sunt scaunele diareice cu sânge și mucus însoțite uneori de dureri abdominale.
Rectoragia este un semn comun în CU. Caracteristicile sângerărilor rectale sunt determinate de localizarea bolii. Cel mai frecvent, pacienții cu proctită acuză emisia de sânge roșu, fie separat de materii fecale, fie la suprafața acestora. Aspectul scaunului este normal, ceea ce pretează la confuzii cu boala hemoroidală. Spre deosebire de boala hemoroidală, pacienții cu colită ulcerativă limitată la rect emit un amestec de sânge cu mucus și pot fi chiar incontinenți. Când boala este extinsă cranial de rect, sângele este amestecat cu materiile fecale și uneori puroi îmbrăcând aspectul de diaree sanghinolentă.
Diareea apare la majoritatea pacienților cu boală extinsă. Până la 30% dintre pacienții cu proctită și procto-sigmoidită nu acuză diaree, ci dimpotrivă constipație. Mecanismele fiziopatologice ale diareei sunt complexe dar primează incapacitatea mucoasei afectate de a reabsorbi sărurile și apa din scaun. Apariția scaunelor diareice influențează starea generală și agravează deficitul ponderal. Pacienții prezintă scaune frecvente (4-15/zi) cu aspect păs¬tos, moale sau rectoragii. Frecvent se asociază inapetență, grețuri, vărsături, febră, scădere ponderală.
Durerea abdominală are caracter de crampă, colică abdominală sau disconfort în etajul abdominal inferior, este însoțită de tenesme rectale și este calmată de emisia scaunului.
Examenul clinic nu evidențiază date semnificative pentru diagnostic în formele ușoare și medii. Uneori palparea profundă a abdomenului poate decela colonul descendent și sigmoidul sub forma unui cordon rigid. În formele severe starea generală este influențată. Pacienții sunt palizi, anemici, febrili, subponderali. Abdomenul este destins de volum, meteorizat, prezintă timpanism la percuție și este dureros la palpare. Instalarea megacolonului toxic (complicație gravă a CU) determină apariția apărării musculare care exprimă interesarea tunicii seroase și iminența perforației.
Pacienții cu CU severă prezintă frecvent manifestări extradigestive, majoritatea acestora fiind comune cu BC.
Explorările biologice sunt nespecifice și exprimă severitatea sângerării și a procesului inflamator. Anemia se datorează inflamației cronice, pierderilor repetate de sânge care antrenează deficit de fier sau malab¬sorbției vitaminei B12. Leucocitoza cu devierea la stânga a formulei leucocitare, creșterea VSH, și a proteinei C reactive se întâlnesc în formele grave, febrile de boală. În puseele de activitate se poate asocia trombocitoză, eozinofilie și monocitoză. Tulburările electrolitice (hipokalie¬mia, hipomagneziemia) se datorează pierderilor prin scaune diareice. Hipocalcemia este secundară atrofiei mucoasei intestinale și tulburărilor în absorbția vitaminei D în BC cu afectare a intestinului subțire. În formele severe, extinse de boală se întâlnește hipoalbuminemie determinată de malabsorbția aminoacizilor și de enteropatia cu pierdere de proteine. Tulburările în absorbția și recircularea sărurilor biliare datorate mucoasei intestinale inflamate pot antrena grade variabile de steatoree. În formele cu manifestări extra¬in¬tes¬tinale hepatobiliare pot apare creșteri moderate ale nivelului enzimelor de colestază. Gamaglobulinele și imunoglobuline¬le serice cresc în fazele de acutizare și revin la normal în perioadele de acalmie a bolii.
Examenul scaunului este util atât pentru diagnosticul pozitiv (evidențiază polimorfonuclearele neutrofile, eozinofile și hematii), cât și pentru diferențierea de infestările parazitare sau de enterocolitele infecțioase (sunt necesare coproculturi pentru Salmonella, Shigella, Campylobacter, Yersinia și determinarea toxinelor produse de Clostridium difficile). Calprotectina fecală (o proteină cu rol antibacterian și antiviral care se găsește în citoplasma PMN) este foarte utilă în diagnosticul diferențial între o patologie funcțională și una organică cu leziuni intestinale.
Tușeul rectal este necesar pentru excluderea unei patologii locale (hemoroizi, cancer anorectal) care poate evolua cu simptomatologie asemănătoare bolilor inflamatorii intestinale.
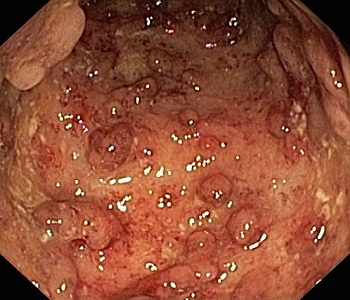
Colonoscopia cu biopsie este explorarea care stabilește diagnosticul de certitudine. În BC, rectosigmoidoscopia poate fi normală la 75% dintre pacienți. Criteriul endoscopic esențial pentru diagnostic este prezența zonelor de mucoasă intactă între ulcerații cu aspect de “pietre de pavaj” (Figura 1). Leziunile sunt segmentare și nu cuprind întreaga circumferință a intestinului afectat. Se pot evidenția ulcerații de dimensiuni mici, eroziuni aftoide, fisuri profunde sau longitudinale, iar la pacienții cu evoluție îndelungată depresiuni pseudodiverticulare, stenoze și pseudopolipi. Sunt necesare biopsii endoscopice etajate care permit diferențierea de colita ulcerativă și evidențiază la 30-50% dintre pacienți granuloame asemănătoare celor întâlnite în sarcoidoză. Biopsiile profunde sunt necesare chiar în prezența unei mucoase aparent normale deoarece permit decelarea leziunilor granulomatoase localizate în submucoasă.
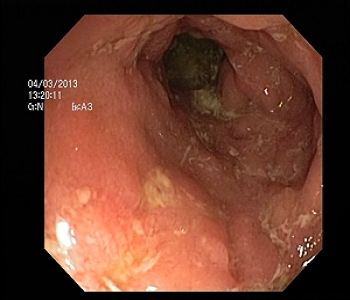
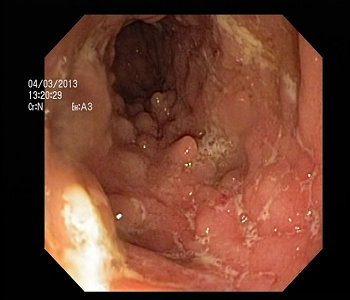
În CU, recto-sigmoidoscopia este de cele mai multe ori suficientă pentru diagnosticul bolii aflată în puseu evolutiv. Colonoscopia totală este necesară doar în fazele de remisiune pentru aprecierea extensiei leziunilor. Este utilă și vizualizarea porțiunii terminale a ileonului pentru diagnosticul diferențial cu BC.
În stadiile precoce de boală, mucoasa intestinului apare hiperemică, edemațiată, cu pierderea desenului vas¬cular (Figura 2a). Ulterior mucoasa devine granulară, friabilă, sângerează ușor la atingerea cu endoscopul; în evoluție apar ulcerații și hemoragii spontane, punctiforme (Figura 2b). Stadiile avansate se caracterizează endoscopic prin apariția pseudo-polipilor pe o mucoasă palidă, subțire, atrofică (Figura 2c). Caracteristic pentru CU este caracterul difuz, uniform al leziunilor, fără zone de mucoasă normală. Biopsia endoscopică cu examenul histologic al fragmentelor recoltate evidențiază prezența infiltratului inflamator și a celorlalte modificări prezentate anterior.
Cromoendoscopia și tehnicile endoscopice noi (endoscopia în mod Narrow Band Imaging, autofluorescența endoscopică etc.) au rolul unei mai bune detecții și caracterizări a leziunilor. Endomicroscopia confocală laser permite evaluarea detaliilor microscopice în timp real, în momentul efectuării endoscopiei atât pentru un diagnostic de certitudine, cât și pentru supravegherea pacienților și detecția precoce a cancerului colorectal.
Examenul radiologic este util pentru aprecierea severității și extinderii leziunilor intestinale. În BC, irigografia cu dublu contrast evidențiază prezența leziunilor în focare, ca mici ulcerații transverse sau longitudinale care se pot prelungi în grosimea peretelui intestinal cu apariția de fistule. Peretele intestinal este îngroșat datorită edemului iar lumenul este îngustat (“semnul coardei”). În formele de boală cu interesarea intestinului subțire, examenul radiologic evidențiază dispariția lizereului mucoasei, rigiditatea segmentelor afectate (prin edem și stenoze) și aspectul caracteristic de “pietre de pavaj” prin interesarea submucoasei în procesul inflamator. În CU, examenul radiologic baritat este util în lipsa explorării endoscopice pentru aprecierea severității și extinderii leziunilor colonice. Examinarea este contraindicată în megacolonul toxic. În stadiile inițiale ale CU, aspectul irigografiei poate fi normal. Odată cu apariția edemului, mucoasa se îngroașă are aspect fin granulat, contur neregulat, irigografia cu dublu contrast poate evidenția ulcerațiile superficiale sub forma unor spiculi marginali. Ulcerațiile profunde dau aspectul radiologic de “buton de cămașă”. În faza de rezoluție, ulcerațiile dispar și se observă pseudopolipii inflamatori sub forma unor mici imagini lacunare diseminate.
Endoscopia digestivă superioară este utilă în evaluarea pacienților cu BC. Implicarea tractului digestiv superior (esofag, stomac și duoden) apare la aproximativ 13% dintre pacienți. Biopsia efectuată din zonele afectate la nivelul tubului digestiv superior evidențiază mult mai frecvent granuloamele decât în cazul leziunilor colonice. La pacienții cu colită nedeterminată, implicarea tractului digestiv superior stabilește diagnosticul de BC. Cel mai frecvent apariția leziunilor la acest nivel nu este izolată și este însoțită de localizarea ileală sau colonică.
Enteroscopia cu balon, cu dublu balon sau enteroscopia spirală are un rol important în evaluare integrală a tractului digestiv și aprecierea severității bolii.
Capsula endoscopică permite examinarea minim invazivă a mucoasei intestinului subțire în scopul diagnosticului inițial, detecției recurențelor, stabilirii extensiei bolii, a răspunsului la tratament și diferențierii BC de CU cu sensibilitate și specificitate superioare celorlalte metode imagistice. Cele mai importante limitări ale metodei sunt considerate lipsa criteriilor uniforme de diagnostic, imposibilitatea prelevării tisulare sau manevrelor terapeutice și riscul de impactare la nivelul stenozelor. În prezența semnelor și simptomelor de boală stenozantă, examinarea intestinului utilizând capsula endoscopică este contraindicată.
Endoscopia ultrasonografică este utilizată recent pentru diagnosticul afectării transmurale, fistulelor, abceselor și adenopatiilor regionale în special în BC perianală.
Tomografia computerizată poate evidenția îngroșarea peretelui anselor intestinale și permite diferențierea acestora de colecțiile localizate intraabdominal (abcese sau flegmoane).
Diagnosticul BC se bazează pe acuzele persistente coroborate cu aspectul endoscopic și rezultatul examenului anatomopatologic al biopsiei colonice sau de intestin subțiere. Activitatea BC poate fi evaluată prin scorul CDAI (Crohn`s Disease Activity Index) care ia în considerare: numărul de scaune zilnic, durerea abdominală, starea generală, complicațiile extraintestinale, necesitatea utilizării opioidelor pentru diaree, prezența unei mase abdominale palpabile și valoarea hematocritului.
Diagnosticul pozitiv de CU se stabilește prin corelarea tabloului clinic cu explorările paraclinice, în special endoscopia digestivă inferioară și biopsia cu examen histopatologic. Astfel, suspiciunea clinică de diagnostic este fundamentată pe prezența simptomelor caracteristice: diaree muco-purulentă, rectoragii, tenesme rectale, durere abdominală. Formele severe și extinse de CU sunt acompaniate de manifestări sistemice: febră, paloare, deshidratare, scădere ponderală, astenie, stare generală alterată. Leucocitoza, anemia, sindromul inflamator nespecific pot întări suspiciunea de diagnostic.
Aprecierea severității CU se face prin utilizarea clasificării Truelove şi Witts (Tabel 1).
Remisiune
Scaune formate, fără produse patologice (în afara tratamentului cortizonic)CU formă ușoară
1-3 scaune/zi, prezența sângelui intermitent în scaun Fără febră, tahicardie, anemie; VSH<30 mm/hCU formă moderată
Criterii intermediare între forma ușoară şi severăCU formă severă
6 scaune/zi, prezența sângelui la majoritatea emisiilor de fecale, temperatura >37.5°C, AV>90/min, scăderea hemoglobinei cu >75% față de normal, VSH>30 mm/hCU formă fulminantă
10 scaune/zi, prezența sângelui la toate emisiile de fecale, temperatura >37.5°C, AV>90/min, scăderea hemoglobinei cu >75% față de normal, VSH>30 mm/h, pacienți care au necesitat transfuzii de sânge--------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Impune în primul rând diferențierea BC de CU prin coroborarea datelor clinice, imagistice și histopatologice.
În majoritatea cazurilor examenul clinic și acuzele pacienților nu diferă semnificativ în BC față de CU. Din punct de vedere al debutului bolii, simptomatologia este mai zgomotoasă în colita ulcerativă și pacienții se prezintă mai repede la medic. În BC, debutul poate fi lent, insidios, scaunele diareice sau cu sange pot lipsi din tabloul clinic și astfel diagnosticul este întârziat mai multe luni sau chiar ani, când deja devin manifeste complicațiile bolii (stenoze, fistule etc.).
Diferențierea endoscopică a celor două boli inflamatorii intestinale este prezentată în Tabelul 2. Implicarea intestinului subțire tranșează clar diagnosticul în favoarea BC.
Examenul histopatologic nu este patognomonic pentru una dintre cele două boli inflamatorii. Prezența leziunilor segmentare, profunde și a granuloamelor sunt foarte sugestive pentru BC în timp ce afectarea continuă a mucoasei și abcesele criptice înclină diagnosticul în favoarea CU
Caracteristica -> CU -> BC
Distribuția topografică -> strict colonică -> orice segment al tractului GIInteresarea rectală -> obligatorie -> 25-50%
Leziuni continui -> caracteristice -> rar
Leziuni segmentare, “pe sărite” -> nu sunt întâlnite -> caracteristice
Ulcerații aftoide -> rar -> caracteristice
Ulcerații lineare -> nu sunt întâlnite -> caracteristice
Fisuri -> nu sunt întâlnite -> caracteristice
Ulcerații pleomorfe -> caracteristice -> rar
Aspect de “piatră de pavaj” -> nu este întâlnit -> caracteristic
Mucoasa normală între leziuni -> nu este întâlnită -> caracteristic
Îngroșarea peretelui (inflamație transmurală și fibroza) -> nu este întâlnită -> frecvent întâlnită
Stenoze -> scurte, largi, reversibile -> caracteristic
Fistule -> nu sunt întâlnite -> caracteristic
--------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Tuberculoza intestinală poate mima BC atât clinic cât și endoscopic. În prezența tuberculozei pulmonare diagnosticul nu ridică probleme majore. Examenul histologic este cel care poate orienta diagnosticul diferențial între cele două afecțiuni.
La orice episod acut al unei boli inflamatorii intestinale trebuie exclusă o cauză infecțioasă. Salmonella, Shigella, Campylobacter sunt microorganismele care produc cel mai frecvent colite infecțioase. Pacienții cu colită infecțioasă au un debut mult mai rapid al simptomatologiei, predomină durerea abdominală și, de cele mai multe ori, raportează prezența de manifestări asemănătoare la unul sau mai multe persoane cu care au intrat în contact recent. Aspectul endoscopic poate să fie identic în cele două patologii și singurul care poate orienta diagnosticul este examenul histopatologic al piesei de biopsie prelevată endoscopic. Infecția cu Yersinia poate produce enterită, enterocolită sau colită. De obicei se vindecă de la sine după o perioadă mai îndelungată. Coprocultura pozitivă și anticorpii serici pot confirma diagnosticul.
Tratamentul recent cu antibiotice trebuie să ridice suspiciunea de colită pseudomemebranoasă cu Clostridium difficile. Determinarea toxinei bacteriene în scaun este esențială pentru diagnosticul pozitiv și trebuie efectuată inclusiv la pacienții cu boală inflamatorie cunoscută la care apare o exacerbare a bolii. Pacienții cu colită pseudomembranoasă acuză diaree apoasă iar examenul endoscopic pune în evidență prezența de membrane alb-gălbui aderente de mucoasa colică.
Transmiterea sexuală a germenilor patogeni intestinali (Neisseria gonorea, Chlamydia, Herpex simplex și Treponema pallidum) prin practici homosexuale poate determina proctite asemănătoare CU. Creșterea prevalenței infecției HIV a lărgit spectrul germenilor patogeni intestinali cu microorganisme ca Isospora, Cryptosoridium, Mycobacterium avium, Citomegalovirus. Chlamydia este identificată prin examen serologic și culturi, iar infecțiile virale (Citomegalovirus, Herpes simlex) prin cultură virală sau examen histologic al pieselor de biopsie.
Colita amoebiană evoluează cu diaree sanguinolentă apărută brusc la subiecți cu călătorii recente în străinătate (contact infectant). La examenul coprologic se evidențiază Entamoeba histolitica, iar în sânge se constată un titru crescut al anticorpilor antiamoebieni.
Diverticulita acută, colita ischemică, colita de iradiere trebuie luate în considerare ca și cauze non-infecțioase care pot mima un episod de CU. Diverticulita acută afectează cel mai frecvent colonul sigmoid iar debutul este brutal în majoritatea cazurilor. Colita ischemică apare la vârstnici cu patologie cardio-vasculară cunoscută iar colita de iradiere urmează după radioterapia aplicată pentru cancerul uterin sau de prostată.
Colita microscopică include colita colagenă și colita limfocitară. Deși manifestările clinice pot fi asemănătoare cu CU, diagnosticul este facilitat de aspectul normal al mucoasei colonului și examenul histopatologic tipic.
Sindromul de intestin iritabil și cancerul colo-rectal pot avea trăsături comune cu bolile inflamatorii intestinale dar istoricul, examenul clinic și endoscopia facilitează diagnosticul.
BC trebuie diferențiată și de alte afecțiuni care determină inflamație intestinală segmentară (limfoame intestinale, jejunoileita negranulomatoasă, actinomicoza sau aspergilloza intestinală) prin colonoscopie sau enteroscopie cu biopsie și examen histopatologic.
Locale
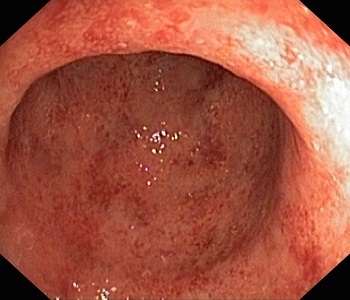
Stenozele intestinale apar frecvent în BC și se datoresc îngustării lumenului intestinal prin fibroză și edem (Figura 3). Inițial stenoza poate fi parțială și intermitentă; ulterior devine completă și trebuie diferențiată endoscopic de stenozele maligne. Clinic pacienții acuză dureri abdominale intense sub formă de colică, cu caracter intermitent sau prezintă tabloul clasic al ocluziei intestinale.
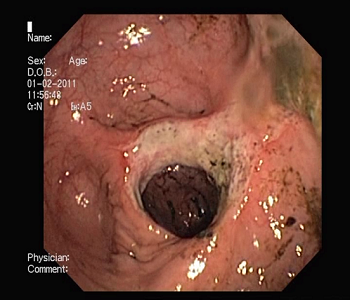
Figura 3: Stenoză strânsă la nivelului colonului ascendent la un pacient cu boală Crohn
Perforația intestinală evoluează clinic cu simtomatologia abdomenului acut chirurgical.
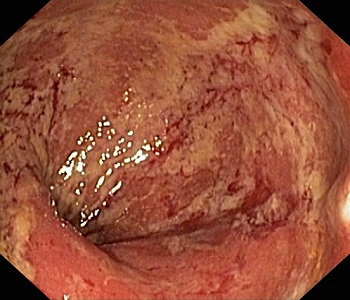
Fistulele cu traiect orb sau cu deschidere în organele cavitare învecinate sunt caracteristice BC (Figura 4). Fistulele între diverse anse intestinale agravează malabsorbția prin by-pass intestinal și reducerea suprafeței absorbtive.
Supurațiile perianorectale apar spontan sau pot fi consecința traumatizării mucoasei anorectale în timpul examenului endoscopic sau irigoscopic. Clinic, pacienții prezintă febră, alterarea stării generale, dureri locale, scaune cu mucus și puroi. Diagnosticul este stabilit în urma tușeului rectal.
Hemoragia digestivă inferioară este o complicație rară dar care poate pune în pericol viața pacientului dacă se instalează brusc și este semnificativă cantitativ.
Dilatația acută a colonului (megacolonul toxic) este o complicație severă care poate apărea încă de la primul puseu în formele fulminante ale CU. Tabloul clinic este dramatic, de abdomen acut chirurgical, cu dureri abdominale intense, meteorism, febră și alterarea rapidă a stării generale. Irigografia sau endoscopia cu insuflație mare de aer sunt contraindicate deoarece pot precipita perforația intestinală. Tratamentul este chirurgical în majoritatea cazurilor.
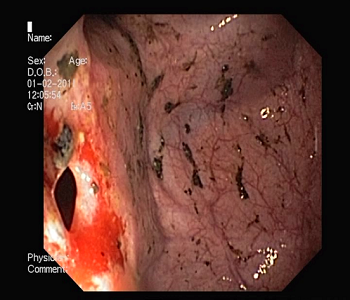
Cancerul de colon are o incidență mai mare la pacienții cu boli inflamatorii intestinale comparativ cu restul populației. Riscul apariției se corelează cu vârsta tânără, evoluția îndelungată a inflamației cronice și extensia procesului inflamator intestinal (frecvență mai mare în pancolitele cu evoluție de peste 10 ani). Frecvența mare de apariție a cancerului de colon la pacienții cu boli inflamatorii intestinale impune controlul periodic endoscopic (la interval de 6-12 luni) pentru depistarea precoce a leziunilor maligne.
Cutaneo-mucoase
• Eritemul nodos apare în puseele de activitate a bolii.
• Pioderma gangrenusum este rară (1-2% dintre pacienți) și se corelează cu activitatea bolii, deși uneori poate persista și în perioadele de acalmie. Erupția cutanată constă în papule și pustule localizate pe trunchi sau membre care se sparg, se ulcerează și pot deveni coalescente. Ulcerațiile au imagini neregulate și se însoțesc în evoluție de necroza epidermului adiacent și a dermului subjacent. Anatomopatologic, pioderma are aspect de abces steril cu infiltrație de polimorfonucleare neutrofile. Cauza este necunoscută.
• Stomatita aftoasă apare la 6-8% dintre pacienți și se poate complica cu suprainfecții cu Candida albicans.
Musculo-scheletice
• Artritele periferice apar la 10-15% dintre pacienții cu boală inflamatorie activă. Interesează articulațiile mari (genunchi, șold, gleznă, umăr), au caracter fluxionar și asimetric. Articulațiile afectate sunt tumefiate, calde și dureroase. Artrita este neerozivă, cedează în perioadele de acalmie a bolii intestinale și frecvent se însoțește de tenosinovită.
• Sacroileita se întâlnește la 12-15% dintre pacienți. Este asimetrică, unilaterală și se traduce clinic prin dureri spontane sau la palparea profundă a articulațiilor sacroiliace. Examenul radiologic și imagistica prin rezonanță magnetică evidențiază pensarea spațiului articular și neregularitatea interliniei articulare.
• Spondilita anchilozantă se asociază la un procent mic dintre pacienții care au antigenul HLA-B27 prezent. Predomină la bărbați, dar raportul B/F este mai mic decât în spondilita anchilozantă fără boală intestinală. Durerile articulare pot preceda sau pot să apară după manifestările digestive. Evoluția afecțiunii reumatismale este independentă de cea a bolii inflamatorii intestinale.
Complicații oculare
• Leziunea cea mai comună este uveita care apare în 5-10% din cazuri. Pacienții acuză dureri oculare, fotofobie și vedere încețoșată. Criza acută de uveită poate fi urmată de atrofia irisului cu depozite de pigment în cristalin. În 50% din cazuri uveita poate fi bilaterală.
• Alte complicații oculare mai rar întâlnite sunt: episclerita, irita și keratita cu blefarită.
Complicații hepatobiliare
• Steatoza hepatică este complicația hepatică cea mai frecvent întâlnită la pacienții cu boli inflamatorii intestinale. Se corelează cu activitatea inflamației intestinale și este însoțită de creșteri moderate ale nivelului seric al transaminazelor și fosfatazei alcaline.
• Colangita sclerozantă este o complicație severă apărută în urma inflamației căilor biliare intra- și extrahepatice.
• Pericolangita este complicația hepatobiliară în care se constată histologic inflamație canaliculară, alterări ale țesutului periportal, zone de necroză hepatocitară.
• Hepatita autoimună și ciroza hepatică sunt complicații rare, dar severe care pot influența evoluția pacienților.
Complicații hematologice
• Boala tromboembolică. Incidența emboliilor pulmonare și a trombozelor viscerale este mai mare la pacienții cu boli inflamatorii intestinale. Starea de hipercoagulabilitate se datorează creșterii factorului V, VIII, a fibrinogenului și scăderii antitrom¬binei 3. Anomaliile fibrinolizei constau în scăderea activității activatorului tisular al plasminogenului (t-PA) și creșterii nivelului activatorului plasmatic al urokinazei.
Complicații metabolice
• Scădere ponderală, reducerea masei musculare, tulburări de creștere la copii.
• Tulburări electrolitice (scăderea nivelului seric al Ca2+, Mg2+ și K+ ).
• Hipoalbuminemie (prin nutriție deficitară sau enteropatie cu pierdere de proteine).
• Steatoree prin tulburări în metabolismul acizilor biliari
• Creșterea absorbției intestinale a oxalaților cu apariția litiazei oxalice renale.
• Creșterea litogenității bilei cu riscul apariției litiazei veziculare.
Complicații rare
• Pericardita cu sau fără epanșament
• Amiloidoza hepatică sau renală
Repausul la pat este indicat în formele severe ale bolii.
Regimul igienodietic presupune evitarea alimentelor față de care pacientul prezintă intoleranță și să asigure un aport caloric și proteic crescut. Vor fi excluse din alimentație produsele care stimulează activitatea motorie a colonului și alimentele care pot declanșa diaree de fermentație (laptele).
Pentru corectarea stării de denutriție, în special la pacienții cu BC cu afectarea intestinului subțire, este necesar un aport proteic adecvat. La pacienții cu toleranță digestivă redusă și la cei cu sindrom de malabsorbție nutriția se va realiza parenteral cu preparate perfuzabile care conțin aminoacizi esențiali și vitamine. Dezechilibrele electrolitice se corectează prin perfuzii cu ser fiziologic (1-3 l/zi), clorură de potasiu, bicarbonat de sodiu, calciu, magneziu.
Tratamentul simptomatic vizează combaterea diareei și calmarea durerilor abdominale. Ca medicație antidiareică se folosesc loperamida (Imodium) și anticolinergicele. Corectarea sindromului anemic se face cu transfuzii de sânge izogrup în caz de anemie severă prin sângerare continuă sau prin administrarea preparatelor de fier pe cale parenterală la pacienții cu anemie feriprivă secundară sângerărilor mici și repetate.
Derivații de acid 5-aminosalicilic (5-ASA).
Această clasa medicamentoasă reprezintă prima linie de tratament pentru inducerea remisiunii la pacienții cu CU forma ușoară sau moderată. Preparatele de 5-ASA se clasifică în derivați sulfatați (salazopirina) și non-sulfatați (mesalamina, olsalazina). Sulfasalazina (salazopirina) este formată dintr-o sulfamidă cu acțiune antibacteriană (sulfopiridina) și un anti-inflamator (5-aminosalicilatul). Este condiționată sub formă de comprimate de 500 mg, se absoarbe la nivelul jejunului și ileonului și parcurge circuitul entero-biliar după care ajunge la nivelul colonului. Acțiunea farmacodinamică a salazopirinei se datorează în principal 5-aminosalicilatului care se fixează pe colagenul mucoasei colonice și inhibă sinteza prostaglandinelor implicate în procesul inflamator. Doza terapeutică uzuală este de 4-6 g/zi. Medicamentul poate determina o serie de efecte adverse: cefalee, febră, erupții cutanate, anemie hemolitică care pot duce la întreruperea tratamentului. Majoritatea efectelor adverse se datoresc sulfopiridinei și din acest motiv preparatele mai noi conțin numai 5 aminosalicilat (mesalamină). Se administrează pe cale orală în doză de 2-4 g/zi sau pe cale rectală (supozitoare, clisme terapeutice, spumă intrarectală) și sunt utilizate mai ales în tratamentul de întreținere pentru prevenirea recidivelor în formele medii și severe de boală, în formele necomplicate.
Terapia cortizonică
Se folosește în formele medii și severe de boală sau la pacienții care nu au răspuns la administrarea de 5-ASA. Doza utilizată în practica curentă este de 40-60 mg/zi (echivalent prednison) urmând apoi reducerea sa treptată pe o perioadă de 6-12 săptămâni. Aproximativ 80% dintre pacienți răspund în prima lună de tratament. În formele severe se preferă calea de administrare parenterală (metilprednisolon 60 mg/zi pentru 5-7 zile) după care se continuă cu prednison per os 40-60 mg/zi timp de 4 săptămâni cu scădere ulterioară treptată. Terapia cortizonică nu este adecvată tratamentului pe perioade lungi datorită numeroaselor efecte adverse, cele mai frecvente fiind cele neuropsihice (tulburări emoționale, insomnie) sau cosmetice (acnee, facies cushingoid, hirsutism etc.). Budesonidul în doză de 9 mg/zi, un glucocorticoid cu aceleași efecte digestive locale ca și prednisonul dar cu mult mai puține reacții adverse datorită fenomenului de primă trecere hepatică, este utilizat în terapia de durată a BC.
Antibioterapia
Antibioticele au un rol clar definit în tratamentul complicațiilor infecțioase ale bolii. Sunt utilizate cu succes și pentru tratamentul fistulelor perineale, stricturilor și BC active. Cel mai studiat este Metronidazolul în doze de 20 mg/kgc/zi cu efecte favorabile. Ciprofloxacina (1g/zi) este folosită pe scară tot mai largă. Este demonstrat efectul său benefic, comparabil cu mesalazina în inducerea remisiunii.
Terapia imunomodulatoare
La pacienții cu pusee severe de acutizare la care dozele mari de glucocorticoizi nu reușesc stăpânirea procesului inflamator se pot asocia medicamente imunosupresoare (azatioprina, 6-mercaptopurina, metotrexat, ciclosporina). Azatioprina și 6-mercaptopurina (analogi purinici) se utilizează în doze de 2-2,5 mg/Kgc/zi, respectiv 1-1,5 mg/Kgc/zi dar au frecvente efecte adverse (febră, artralgii, mielodepresie). Metotrexatul (25 mg/săptămână) este considerat o alternativă eficientă pentru pacienții care nu au răspuns sau nu au tolerat tratamentul cu analogi purinici atât în inducerea cât și menținerea remisiunii. Ciclosporina (4 mg/kgc/zi) este un imunosupresor puternic care poate fi utilizat în fazele acute, deși efectele adverse și apariția de noi medicamente imunomodulatoare (Tacrolimus, Mycophenolate mofetil) îi limitează mult utilizarea actuală.
Terapia biologică
Indicațiile actuale includ pacienții care nu au răspuns la tratamentul imunosupresor convențional în doze adecvate sau acest tratament este contraindicat sau a produs reacții adverse care au impus întreruperea sa. Sunt definite profiluri ale pacienților cu probabilitate de răspuns favorabil la terapia biologică (tineri, nefumători, cu durată redusă a afecțiunii, naivi la agenți biologici și imunosupresoare, cu activitate inflamatorie crescută reflectată de valorile crescute ale PCR și VSH, leziuni endoscopice active) sau nefavorabil (vârstnici, fumători, pacienți operați pentru BC, afectare ileală izolată, boală perianală).
Infliximab este primul agent biologic la care s-a demonstrat eficiența în inducerea remisiunii. Este un agent anti TNF-alfa himeric, constituit din anticorpi monoclonali de tip IgG1 (25% murini și 75% umani). Inducția remisiunii se realizează cu trei doze (5mg/kg în perfuzie intravenoasă) administrate la 0, 2 și 6 săptămâni, iar menținerea remisiunii cu doze administrate la 8 săptămâni.
Adalimumab este un agent anti TNF-alfa complet umanizat de tip IgG1. Inducția remisiunii se realizează cu două doze (80-160 mg subcutanat) administrate la 0 și 2 săptămâni iar menținerea cu doze administrate din două în două săptămâni (40-80 mg subcutanat).
Vedolizaumab, agent anti-integrine, a fost deja aprobat spre utilizare. BII se caracterizează printr-o inflamație cronică ce apare o dată cu migrarea mediatorilor inflamatori în organele țintă. Infiltratul limfocitar din lamina propria și procesul de migrare al limfocitelor este coordonat de interacțiunea unor integrine cu molecule specifice de adeziune. Acest mecanism a dus la dezvoltarea vedolizumab. Eficacitatea medicamentului în inducerea și menținerea remisiunii a fost demonstrată în studiile Gemini 1, 2 și 3.
Molecule mici
Aceste molecule administrate oral intervin în semnalizarea celulară și au un beneficiu major comparativ cu medicamentele sub formă de anticorpi, prin costul redus și administrarea orală. Tofacitinib inhibă preferențial semnalizarea celulară prin receptorii heterodimerici ai citokinelor care asociază cu JAK3 și/sau JAK1 cu selectivitate funcțională față de receptorii citokinelor care semnalizează prin intermediul perechilor de JAK2. Această inhibiție atenuează semnalizarea interleukinelor (IL-2, -4, -6, -7, -9, -15, -21) și interferonilor tip I și tip II, ceea ce duce la modularea răspunsului imun și inflamator.
Peste 75% dintre pacienții cu BC vor necesita pe parcursul evoluției timp de 20 de ani cel puțin o intervenție operatorie. Se practică rezecții segmentare în funcție de extensia procesului inflamator dar recidivele bolii sunt frecvente în amonte de anastomozele chirurgicale.
Indicațiile tratamentului chirurgical în BC sunt:
• stenozele intestinale persistente sau fixe care duc la ocluzie intestinală;
• fistulele vezicale, vaginale sau cutanate;
• fistulele sau abcesele perianale care nu răspund la tratamentul medical;
• colecțiile localizate intraabdominal.
În CU, tratamentul chirurgical este indicat în formele fulminante care nu răspund în câteva zile la tratament, în formele cronice severe manifestate prin diaree cronică neinfluențată de medicație și scădere ponderală marcată sau la pacienții cu complicații (perforație liberă în marea cavitate peritoneală, abces pericolonic, hemoragie masivă, megacolon toxic).
Se pot practica mai multe tipuri de intervenții (ileostomie, proctocolectomie cu ileostomie, colectomie subtotală cu ileostomie), dar de cele mai multe ori se preferă colectomia totală cu anastomoză ileorectală.
Megacolonul toxic, complicație majoră a CU, necesită măsuri intensive de terapie pentru a preveni riscul vital. Pacienții vor fi reechilibrați hidroelectrolitic și cardiocirculator prin transfuzii de sânge și perfuzii cu electroliți. Se suprimă alimentația orală și se montează sondă de aspirație nazogastrică. Având în vedere puseul inflamator sever și posibilitatea perforației se recomandă administrarea de antibiotice cu spectru larg în doze mari. Tratamentul patogenic constă în administrarea pe cale intravenoasă în perfuzii de glucocorticoizi. Dacă în 24-48 ore nu se reușește controlul procesului inflamator, persistă riscul perforației și starea generală a pacientului nu se ameliorează este indicată colectomia.
Sergiu Cazacu, Dan Gheonea, Tudorel Ciurea, Ion Rogoveanu, Adrian Săftoiu, Cristin Vere, Medicină internă – Gastroenterologie. Editura Medicală Universitară Craiova, 2015.

